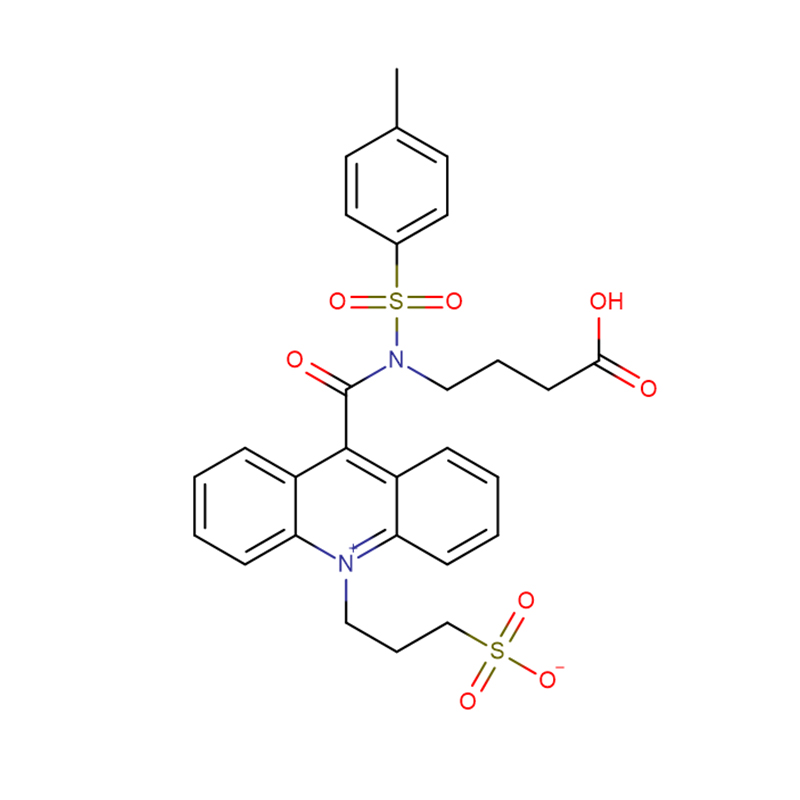
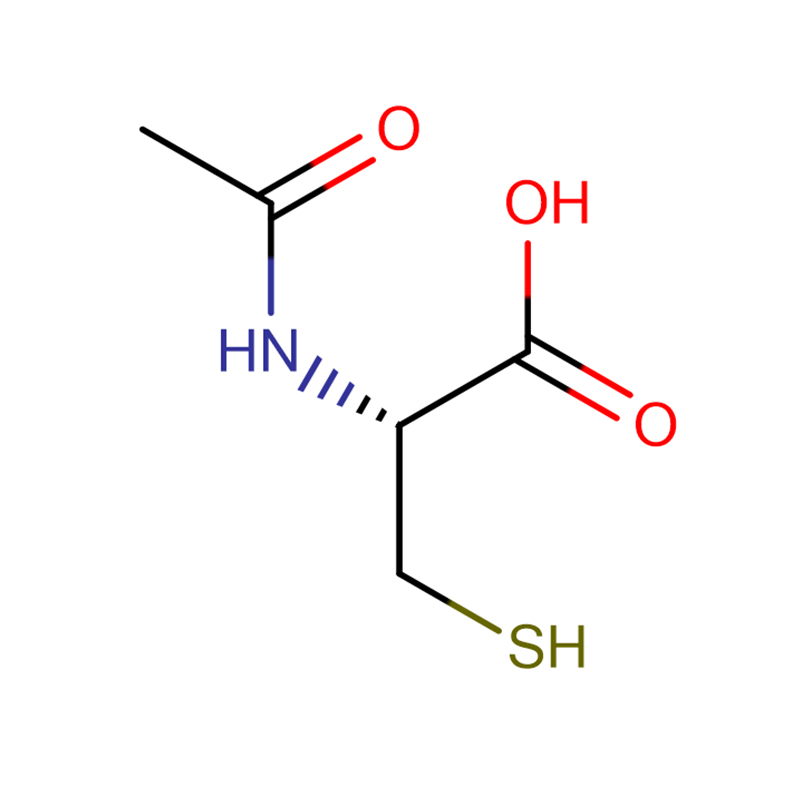
4-Amino-3-hidrazino-1,2,4-triazol-5-tiol Cas:28836-03-5 99% Sólido amarelo a verde
| Número de catálogo | XD90146 |
| Nome do produto | 4-amino-3-hidrazino-1,2,4-triazol-5-tiol |
| CAS | 28836-03-5 |
| Fórmula Molecular | C16H13NO3S·NH3 |
| Peso Molecular | 316,37 |
| Detalles de almacenamento | Ambiente |
| Código Tarifario Harmonizado | 2923900090 |
Especificación do produto
| Aparición | Sólido de amarelo a verde |
| Assay | ≥ 99 % |
| Punto de fusión | 237 °C (dec.) (lit.) |
| Solubilidade | NaOH: soluble 1 N |
| Soluble en auga | Soluble en auga, NaOH 1N e metanol. |
1.Estudamos os efectos inhibidores da isorhamnetina sobre a tirosinase de cogomelos mediante a cinética de inhibición e a simulación computacional.A isorhamnetina inhibiu de forma reversible a tirosinase de forma mixta a Ki=0,235±0,013 mM.As medicións da fluorescencia intrínseca e de unión de 1-anilinonaftaleno-8-sulfonato (ANS) mostraron que a isorhamnetina non induciu cambios significativos na estrutura terciaria da tirosinase.Para coñecer o proceso de inactivación, a cinética calculouse mediante medicións de intervalo de tempo e reaccións continuas do substrato.Os resultados indicaron que a inactivación inducida pola isorhamnetina foi unha reacción de primeira orde con procesos bifásicos.Para obter máis información, simulamos o acoplamento entre a tirosinase e a isorhamnetina.A simulación foi exitosa (enerxías de unión para Dock6.3: -32.58 kcal/mol, para AutoDock4.2: -5.66 kcal/mol e para Fred2.2: -48.86 kcal/mol), o que suxire que a isorhamnetina interactúa con varios residuos, como como HIS244 e MET280.Esta estratexia de predicir a interacción da tirosinase en combinación coa cinética baseada nun composto de flavanona pode resultar útil na selección de posibles inhibidores naturais da tirosinase.
2. A vía de despregamento do ácido da conalbúmina (CA), unha glicoproteína monomérica procedente da clara de ovo de galiña, investigouse mediante espectroscopia CD lonxe e case UV, emisión de fluorescencia intrínseca, sonda de fluorescencia extrínseca 1-anilino-8-naftaleno sulfonato (ANS) e dispersión dinámica de luz (DLS).Observamos cambios dependentes do pH na estrutura secundaria e terciaria do CA.Ten unha estrutura secundaria α-helicoidal nativa a pH 4,0 pero unha estrutura de perda a pH 3,0.O CA existía exclusivamente como estado de glóbulo pre-fundido e estado de glóbulo fundido en solución a pH 4,0 e pH 3,0, respectivamente.O efecto do pH na conformación e termoestabilidade do CA apunta á súa resistencia á calor a pH neutro.Os resultados do DLS mostran que o estado MG existía como forma compacta en solucións acuosas con radios hidrodinámicos de 4,7 nm.A extinción da fluorescencia do triptófano pola acrilamida confirmou aínda máis a acumulación dun estado intermedio, parcialmente despregado, entre os estados nativo e desenvolvido.


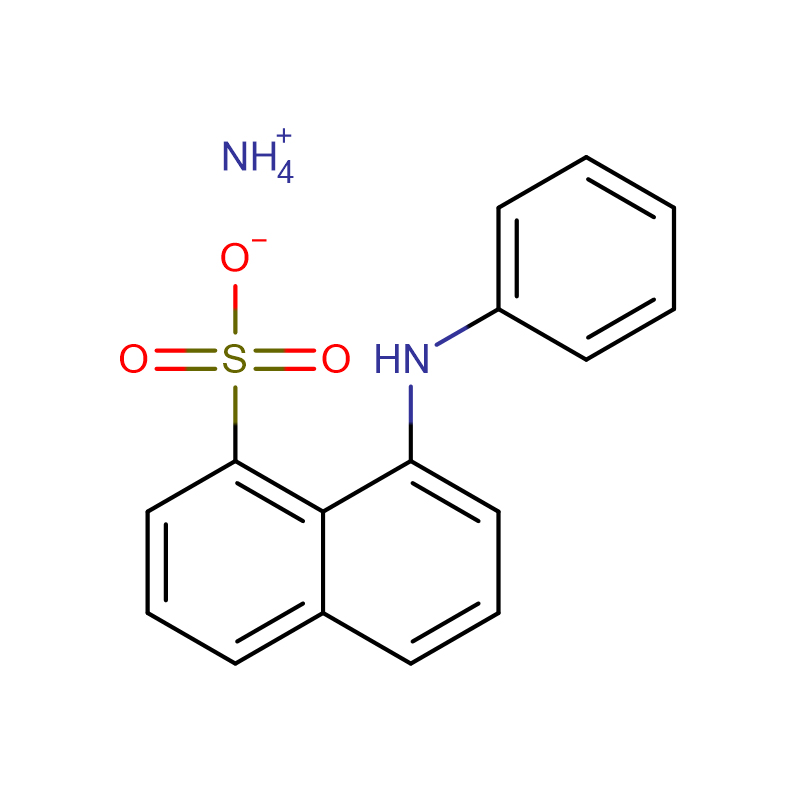


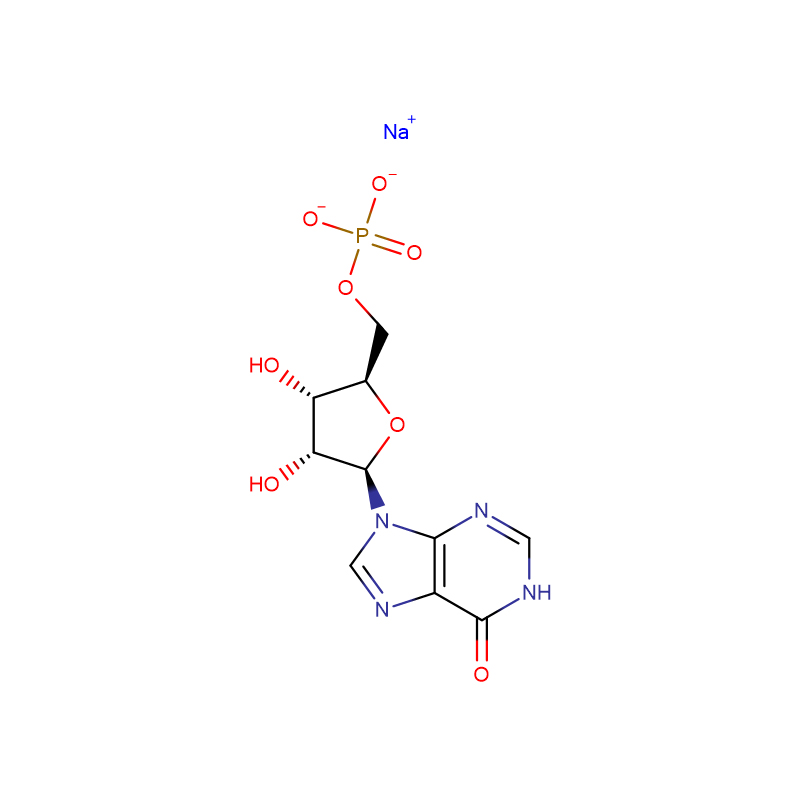
![N-[[bis[4-(dimetilamino)fenil]amino]carbonil] glicina sal sódica Po cristalino de branco a verde grisáceo](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)