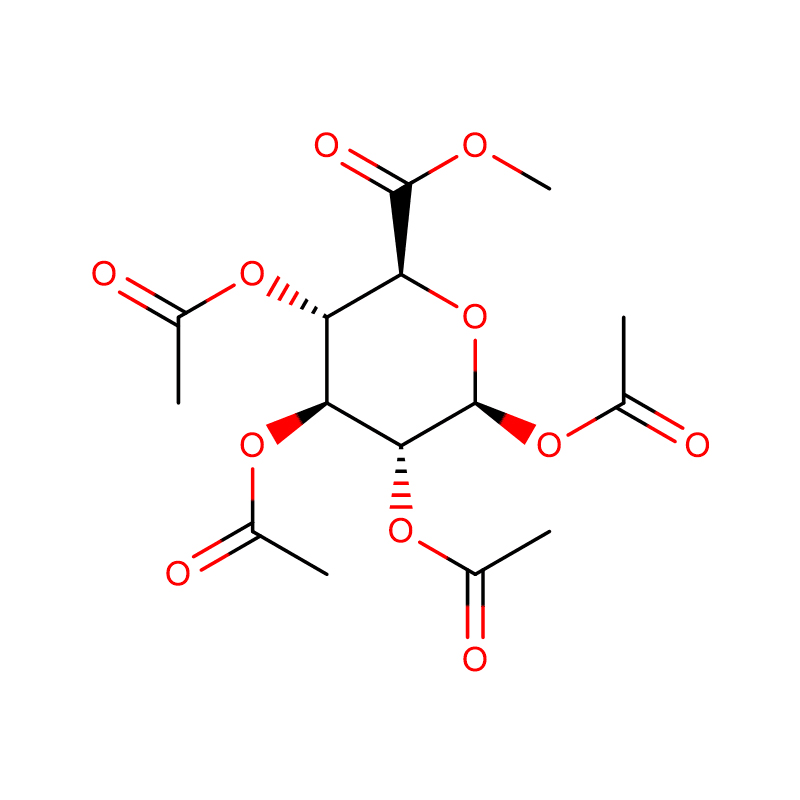
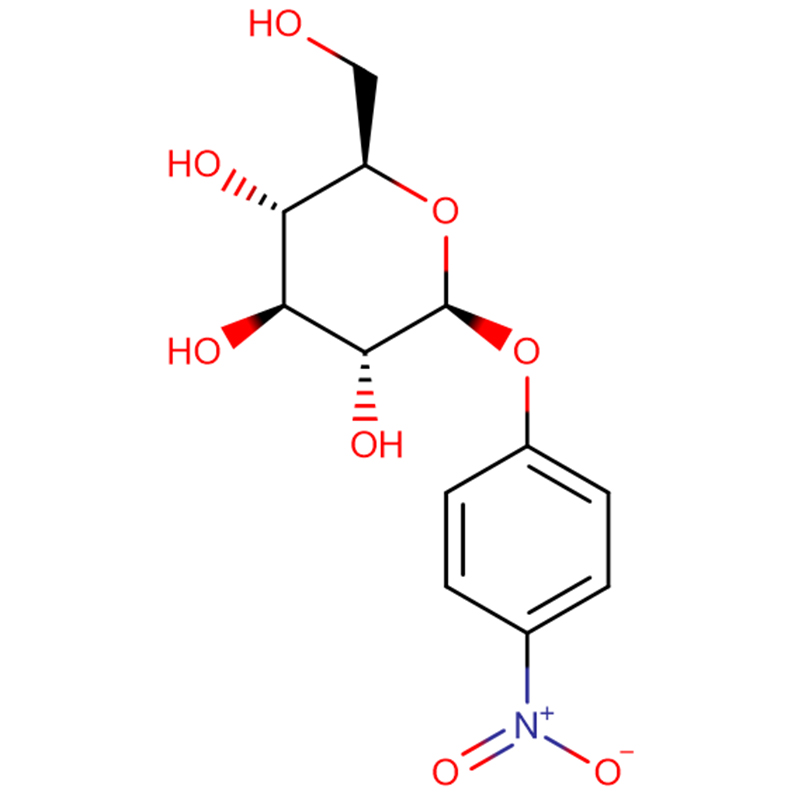
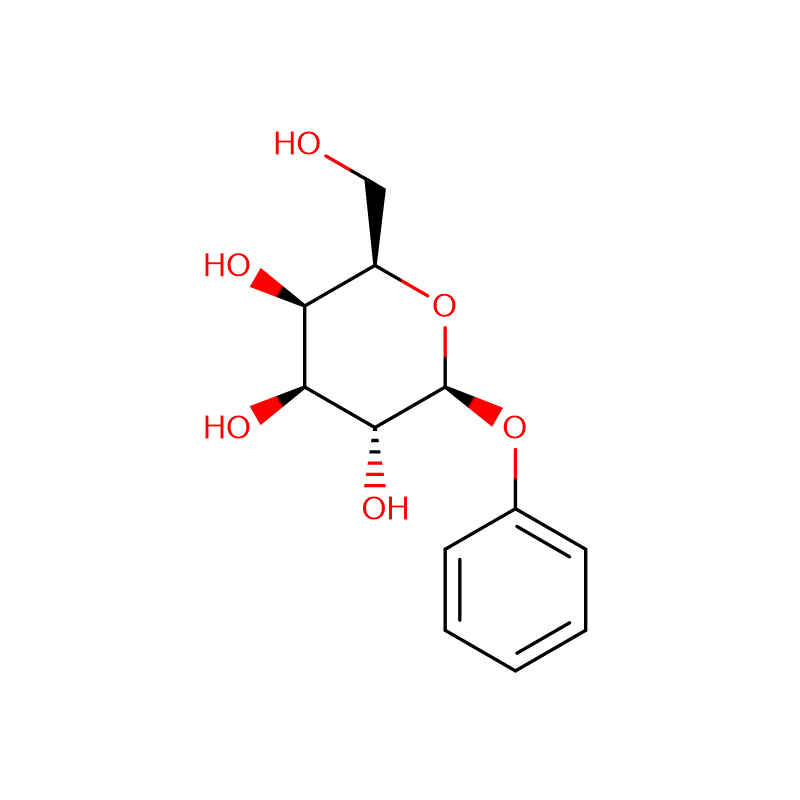
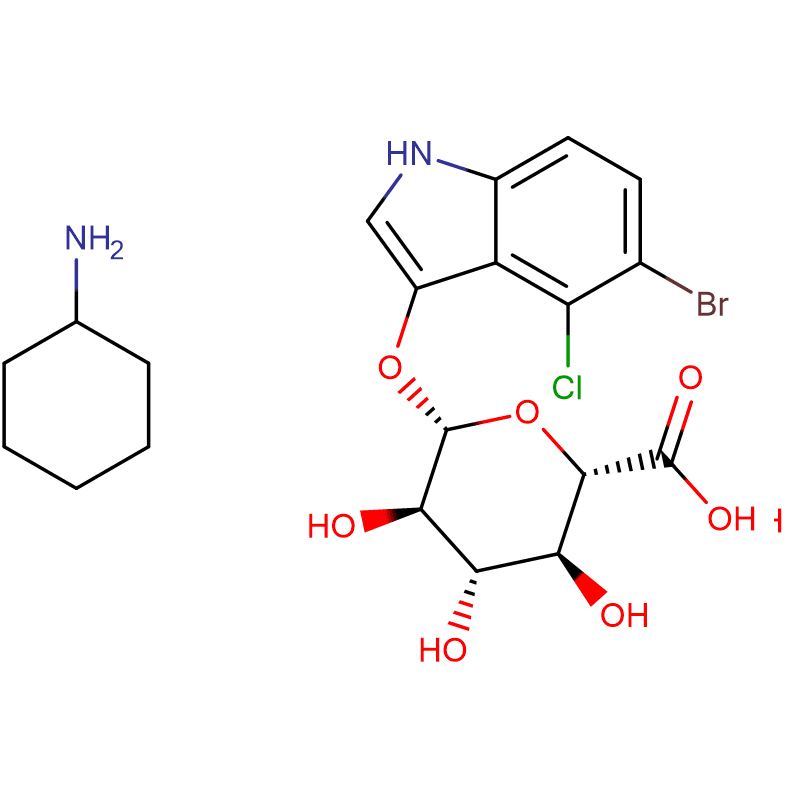
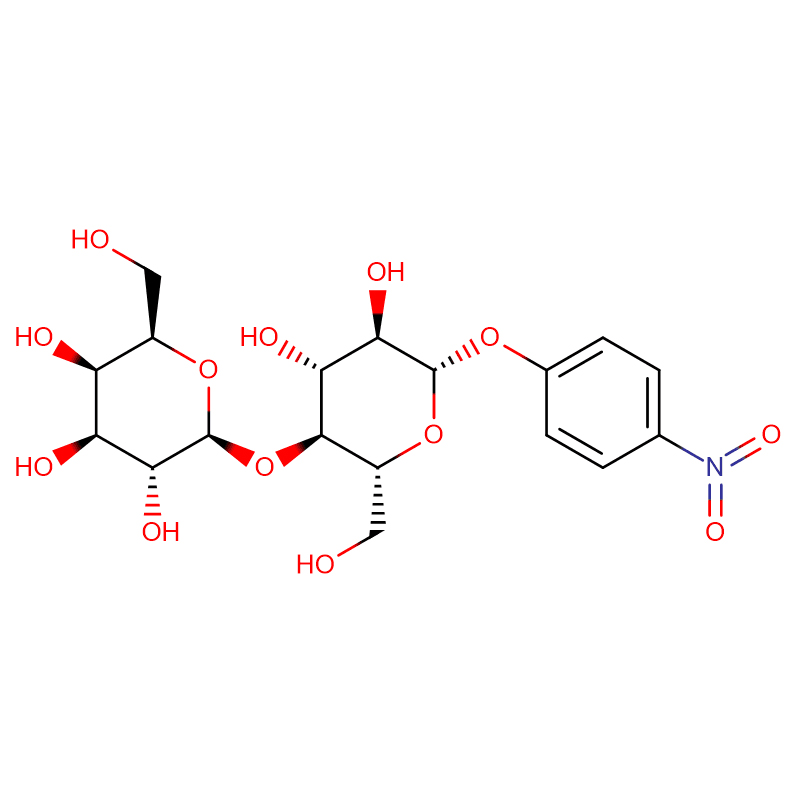
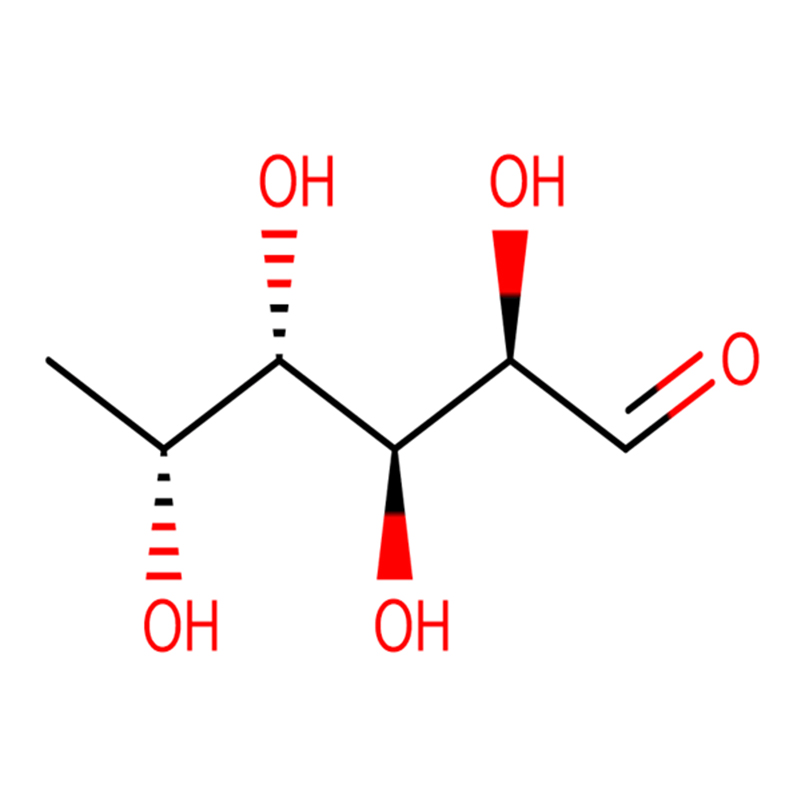
Dous análogos isoméricos do biciclo[4.1.0]heptano do inhibidor da glicosidasa galacto-validamina, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hidroximetil)biciclo[4.1.0]heptano -2,3,4-triol, foron sintetizados en 13 pasos a partir da 2,3,4,6-tetra-O-bencil-D-galactosa.As actividades inhibitorias das dúas aminas restrinxidas pola conformación e as súas correspondentes acetamidas, medironse contra encimas comerciais de alfa-galactosidasa do gran de café e de E. coli.A actividade do encima GH27 da familia glicosil hidrolasa (gran de café) foi inhibida competitivamente pola 1R,6S-amina (7), unha interacción de unión que se caracterizou por un valor K(i) de 0,541 microM.A alfa-galactosidase de E. coli GH36 mostrou unha interacción de unión moito máis débil coa 1R,6S-amina (IC(50)= 80 microM).A diastereoisómera 1S,6R-amina (9) uniuse débilmente a ambas galactosidases, (gran de café, IC(50)= 286 microM) e (E. coli, IC(50)= 2,46 mM).