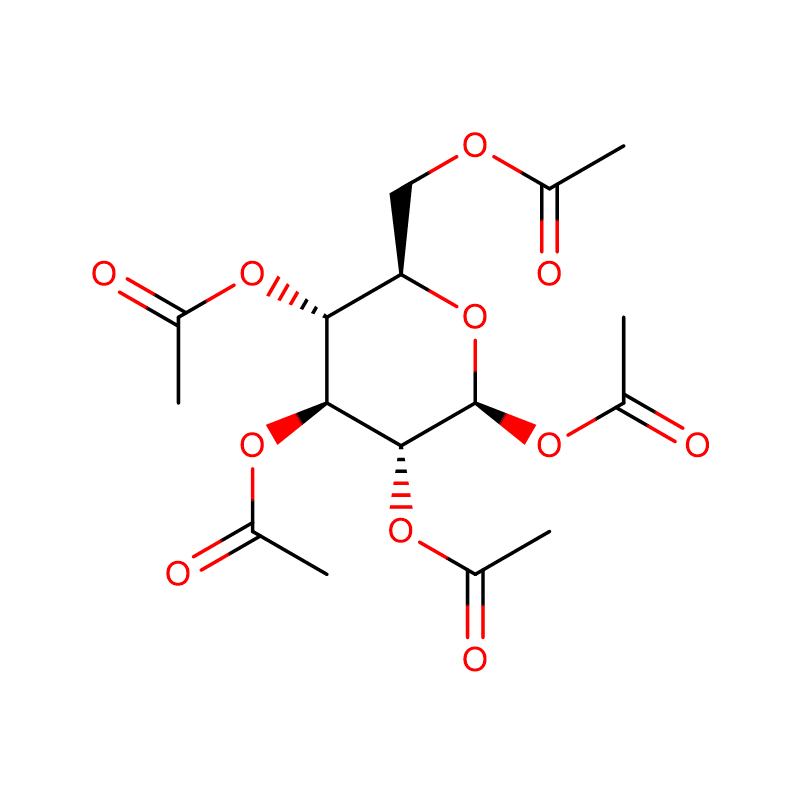
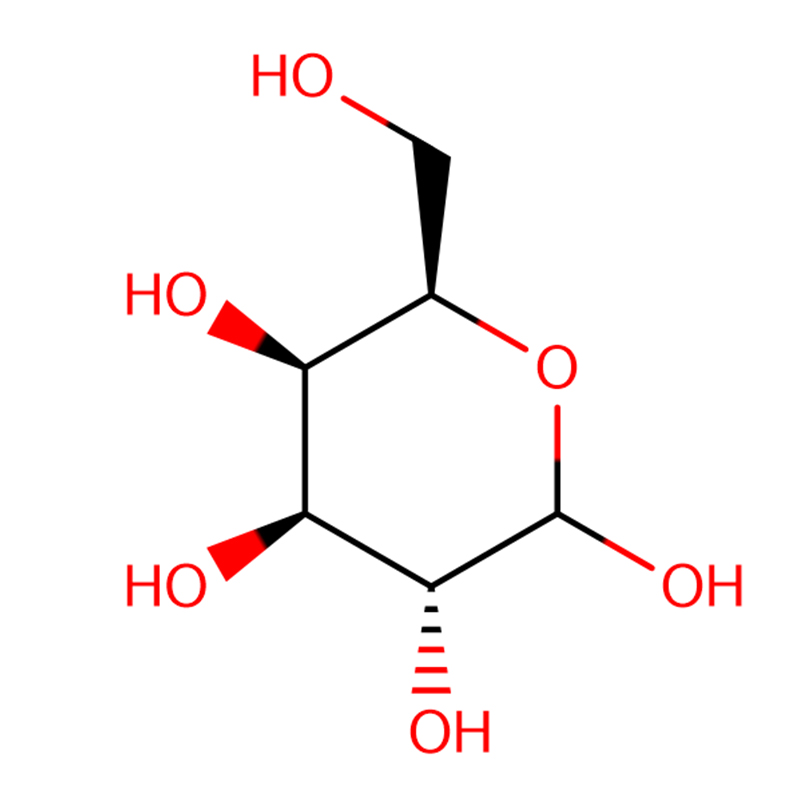
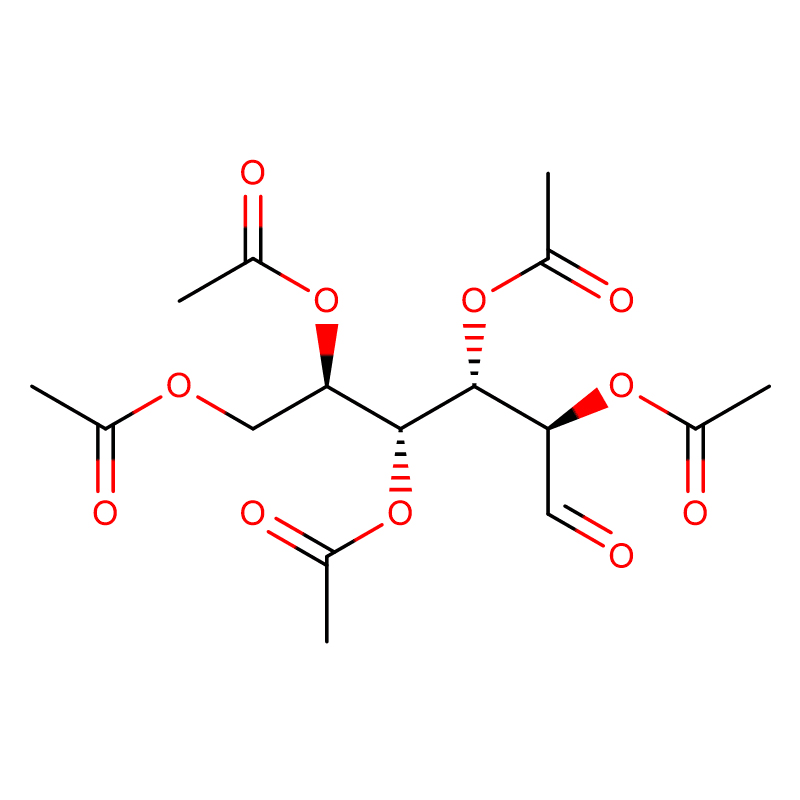
4-NITROFENIL-ALFA-D-MANOPIRANÓSIDO CAS: 10357-27-4 Po blanquecino 98%
| Número de catálogo | XD90011 |
| Nome do produto | 4-Nitrofenil-alfa-D-manopiranósido |
| CAS | 10357-27-4 |
| Fórmula Molecular | C12H15NO8 |
| Peso Molecular | 30301.25 |
| Detalles de almacenamento | -2a -8°C |
| Código Tarifario Harmonizado | 29400000 |
Especificación do produto
| Auga | <5% Karl Fische |
| Solubilidade | O 1% en DMF é claro e incoloro |
| Pureza | 4-nitrofenol libre <200 ppm |
| HPLC | >98% |
| Aparición | Po blanquecino |
Insights mecanicistas sobre unha familia de alfa-manosidases dependente de Ca2+ nun simbionte intestinal humano.
As bacterias do colon, exemplificadas por Bacteroides thetaiotaomicron, xogan un papel fundamental no mantemento da saúde humana ao aproveitar grandes familias de glicósidos hidrolases (GHs) para explotar polisacáridos dietéticos e glicanos hóspedes como nutrientes.Tal expansión da familia GH é exemplificada polas 23 glicosidases da familia GH92 codificadas polo xenoma de B. thetaiotaomicron.Aquí mostramos que se trata de alfa-manosidases que actúan mediante un único mecanismo de desprazamento para utilizar N-glicanos hóspedes.A estrutura tridimensional de dúas manosidases GH92 define unha familia de proteínas de dous dominios na que o centro catalítico está situado na interface do dominio, proporcionando asistencia ácida (glutamato) e base (aspartato) para a hidrólise nun Ca(2+)- xeito dependente.As estruturas tridimensionais dos GH92 en complexo con inhibidores proporcionan información sobre a especificidade, o mecanismo e o itinerario conformacional da catálise.Ca(2+) xoga un papel catalítico clave para axudar a distorsionar o manósido lonxe da súa conformación da cadeira de estado fundamental (4)C(1) cara ao estado de transición.(Bibliografía: Nat.Chem.Biol.6, 125-32, (2010)
Cromatografía de afinidade frontal de glicoasparaxinas de ovoalbúmina nunha columna de concanavalina A-sefarosa.Un estudo cuantitativo da especificidade de unión da lectina.
As interaccións da concanavalina A (ConA) inmovilizada con Sepharose 4B con 10 glicoasparaxinas derivadas da ovoalbúmina foron investigadas cuantitativamente mediante cromatografía de afinidade frontal.Neste método, unha solución de hidratos de carbono aplícase continuamente a unha columna de ConA-Sepharose e o retardo da fronte de elución mídese como un parámetro da forza da interacción.Pódese determinar a constante de disociación (Kd) para cada sacárido con ConA.Unha análise da unión do p-nitrofenil-alfa,D-manósido demostrou que as propiedades de unión de ConA non cambian esencialmente despois da inmobilización en Sepharose 4B.Cada unha das glicoasparaxinas de ovoalbúmina foi marcada con tritio polo método de metilación redutiva para a súa análise.Unha comparación dos valores de Kd obtidos mostrou que a unión de ConA varía considerablemente con diferenzas estruturais moi leves da cadea de glicosilo.Os resultados suxiren que ConA recoñece unha estrutura específica de cadea de glicosilo, Man alfa 1-6(Man alfa 1-3)Man, na que polo menos un grupo hidroxilo na posición C-3 da manosa unida a C-6 debería estar libre.